 11
11
个人防护类防护服属于Ⅲ类产品,需要公告机构介入,应遵循以下流程才能满足出口欧盟的准入条件:
① 企业需将产品送到公告机构实验室进行型式检测;
② 编制产品技术文件;
③ 结合PPE法规建立体系;
④ 完成公告机构现场审核,即可获得书。
SUNGO有丰富的欧盟注册经验。SUNGO实验室可以开展隔离衣、手术衣的性能测试和验服务,助力客户产品顺利上市欧盟市场保驾**。
法规条款增加,认评审更加严格
a. 分类规则增加:由MDD的18条增加到 22条;
b. 基本要求检查表条目增加:由MDD的13条增加到 MDR的23条;
c. CE技术文件的结构发生了变化,分为:产品技术文件和上市后文件(MDD只要求产品技术文件);
d.评价报告。MDR要求企业提供*四版评估报告,相比于*三版,*四版要求更为严格;
5:MDR要求更高的透明度和可追溯性
a. 引入了器械标识UDI,增加产品的可追溯性;
b. 企业的相关信息都会被收集到欧洲器械数据库(EUDAMED);
c. 建立上市后监督(PMS)系统;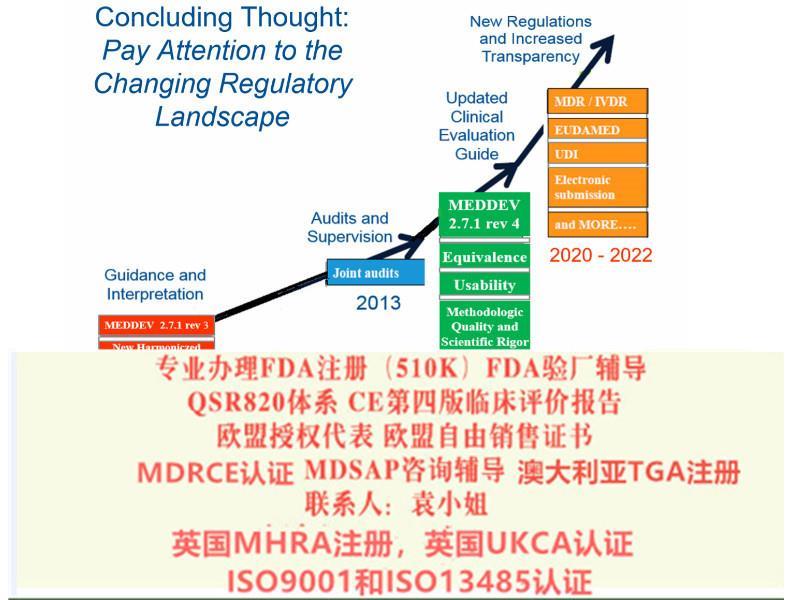
主管机构应制定年度活动计划,并分配足够数量的胜任人力和物质资源以执行这些活动。
ISO 17664的规定适用于用于侵入性或其他直接或间接接触患者的设备。ISO 17664中没有定义处理指令,相反,ISO 17664规定了一些要求,以协助器械制造商提供详细的加工说明,包括下列活动(如适用):
a) 使用时的初始处理;
b) 清洗前准备;
c) 清洁;
d) ;
e) 干燥;
f) 检查和维修;
g) 包装;
h)
i) 存储
j) 运输
需要办理以下认可以随时找我 :
1:出口欧盟:MDR CE认/IVDRCE认,欧盟授权代表,欧盟注册,欧盟自由销售书
2:出口英国:英国代表,英国MHRA注册,UKCA认,英国自由销售书
3:出口美国:美国FDA注册,FDA510K,QSR820体系
4:中国:国内的器械注册和生产许可
5:出口加拿大:加拿大的MDEL注册
6:质量管理体系认:ISO13485咨询和认
① 选择具有MDR审核的公告机构,提交认申请,签订认合同;
② 建立符合欧盟法规和EN ISO13485:2016标准要求的体系;
③ 按照MDR附录II+附录III的要求编制CE技术文件;
④ 欧盟授权代表,签署《欧代协议》;
⑤ 公告机构对产品技术文件进行预审;
⑥ 完成公告机构现场审核及审核中不符合项的整改;
⑦ 公告机构颁发CE书
⑧ 欧盟授权代表在欧洲进行产品注册。
欧盟国家出具的自由销售,目前对器械做的比较多的是欧盟成员国的局出具的自由销售。SUNGO SUNGO Europe B.V. 可以办理。
http://sungofda.cn.b2b168.com
欢迎来到上海沙格企业管理咨询有限公司网站, 具体地址是上海市金山区石化街道松南支路48号-826座,联系人是袁小姐。
主要经营上海沙格企业管理有限公司SUNGO是欧盟授权代表,从事FDA验厂、欧盟自由销售书、医疗器械单一体系审核MDSAP、CE*四版临床评价报告、MDRCE认、CE MDR认、CE技术文件、EU 2017/745认、MDEL注册、MDR、CE认等服务。。
单位注册资金单位注册资金人民币 100 万元以下。
我们公司主要提供CE,MDR认,MDR,CE认,IVDR,欧代,EU2017/745认,2017/746,EC,REP,CE技术文件,CE*四版临床评估报告.SUNGO,EN,455,UK,EN12184,清洗验,FDA验厂等服务,我们确信,凭借我们的专业服务和良好的协调、沟通能力,使客户在经营生产中顺利进行,协助客户不断成长,在合作中与客户实现共赢。欢迎您致电咨询!