周期4周
包装纸质
品牌SUNGO
是否进口否
可售卖地**
SUNGO将秉承一贯“服务、客户”的原则,依托的技术团队,优化我们的服务,让更多的器械合法、*进入市场,为器械行业健康发展贡献力量。
因为,所以放心!
Class I:
1. 为申请Medical Device Establishment License (MDEL)准备相应的技术文件
2. 提交MDEL申请,支付行政收费。
3. 申请评审通过,将在Health Canada网站公示。
Class II:
1. 通过CMDCAS认可的认证机构进行ISO 13485 审核认证(体系审核除ISO13485要求外还要包括CMDR的要求),获得证。
2. 准备Canadian Medical Device License (MDL)申请。
3. 提交MDL申请,并交纳行政收费。
4. Health Canada评审MDL申请, 评审通过后进行网站公示。
SUNGO SUNGO Europe B.V. 总部位于荷兰,提供技术服务。主要业务是根据欧洲立法和国际标准,为客户提供完整的技术解决方案。SUNGO集团凭借**网络和队伍为**客户提供法规,在器械行业尤为专长。提供欧盟授权代表服务,可以为客户减少中间环节,节约时间和费用,使您的产品在符合现行欧盟法规的情况下进入市场的程序简单化。
SUNGO SUNGO Europe B.V.作为欧盟代表是被荷兰国家局局认可的。可以帮企业到欧盟主管注册,以免进入海关时出问题和引起法律纠纷,造成不必要的经济损失。
欧盟国家出具的自由销售,目前针对器械做的比较多的是欧盟成员国的局出具的自由销售。

目前急需做CE认证的客户很多,检测认证公司,代理公司也是鱼目混
杂,参差不齐。
怎么辨别口罩CE认证的真假呢?
1,凡是说3、5两千可以出CE证的都是
2,凡是说3/2天可以*的都是
3,凡是说国内公司自己可以发CE证的都是
辨别证的真伪很重要,因为一旦货到了港口清不了关损失就大了。
所以不要贪图*和快而上当受
NB号的CE证。按照现行的欧盟器械法规,此路径获取CE证的
时间至少8个月以上,费用比较昂贵。
欧盟I类器械,如果是非灭菌产品,具体分类为I类。按照指令要求,
公告机构不可强制介入I类器械的发证事宜,制造商可以基于完整的CE技
术文档宣称符合CE(自我CE符合性声明格式如下)。也即,制造商不需
要找发证机构去申请带NB号的CE证,制造商根据自己出具自我CE符
合性声即可打上CE mark,出口欧盟。在欧盟有经销活动前,需要委托
欧盟授权代表去当地主管机构做欧盟注册,整个欧盟28个成员国,只需
登记一次。整个周期是1-4周。
---签订欧盟代表协议---起草I类器械的MDR CE技术文档---欧盟注册---
签发DOC。
这种途径符合CE的标志,就是完成如上四步,终生效的DOC是没有公
告号的。
建议企业同步建立ISO 13485器械质量体系,产品需要满足的检测
要求(比如口罩的EN14683产品性能检测;ISO 10993生物相容性检
测,还是要满足)。产品市场后的监督工作还是要有计划做。
另外,外销产品随附的文件,如说明书、标签都是要符合欧盟相关
器械标准要求EN ISO 15223 & EN 1041。
现在市面上所有发的设计精美,各式各样的所谓的发证机构发出的证
书,费用在1-2万,周期几天的,这种证,其实只是精装的DOC,如
果没有有效的欧代协议+TCF技术文档+欧盟注册作为支撑,这种证是
没有支撑证据的,也即没有真实的作用。

我们该怎么办?
l 重新确认产品风险分类等级,确认是否有风险等级升级的情况?
例如部分可重复使用的器械,原属于ClassⅠ的器械,按照新法规变成了ClassⅠ*类器械。美容类产品原MDD下不属于范围,现MDR法规中已纳入;
l 确认原CE证的发证机构是否已获得欧盟当局批准的颁发MDR证的,目前拥有该的认证机构:BSI、TUV南德(注意TUV莱茵目前还未获得批准);
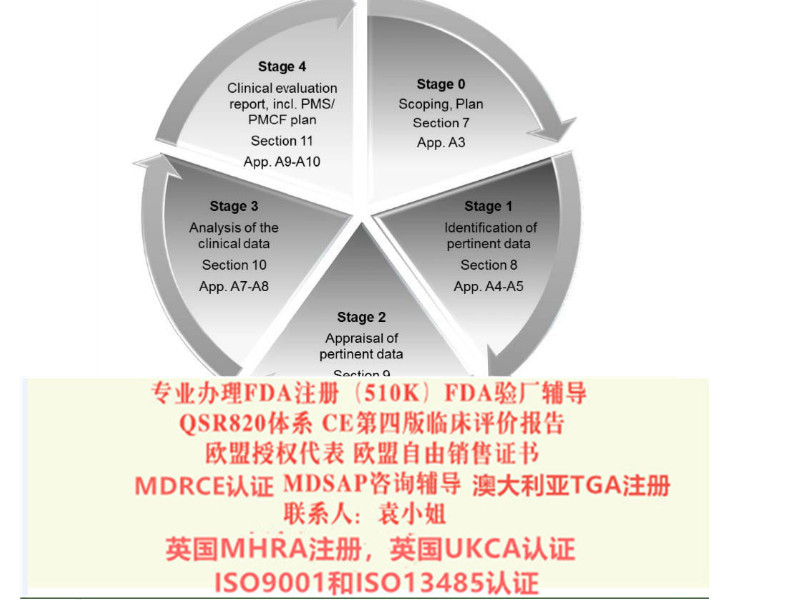
l 确认原CE认证时的技术文件中是否含有按照Rev4原则提供的评价报告;
l 确定企业合规负责人(MDR法规要求),有相应能力、和经验来承担相应的法规工作职责。
l 修改原CE技术文件,建立质量管理体系,向具有MDR发证的认证机构提出MDR-CE认证申请,获得MDR法规下的新CE证。
SUNGO可以在过渡期内为提供新旧法规的咨询服务,包括:
协助判定产品分类
协助选择合理的符合性途径
协助选择合适的认证机构
制定认证的解决方案
协助完成评估
编写CE技术文件
欧盟代表服务
http://sungofda.cn.b2b168.com