产地上海
可售地**
品牌SUNGO
型号SUNGO BV
包装纸质
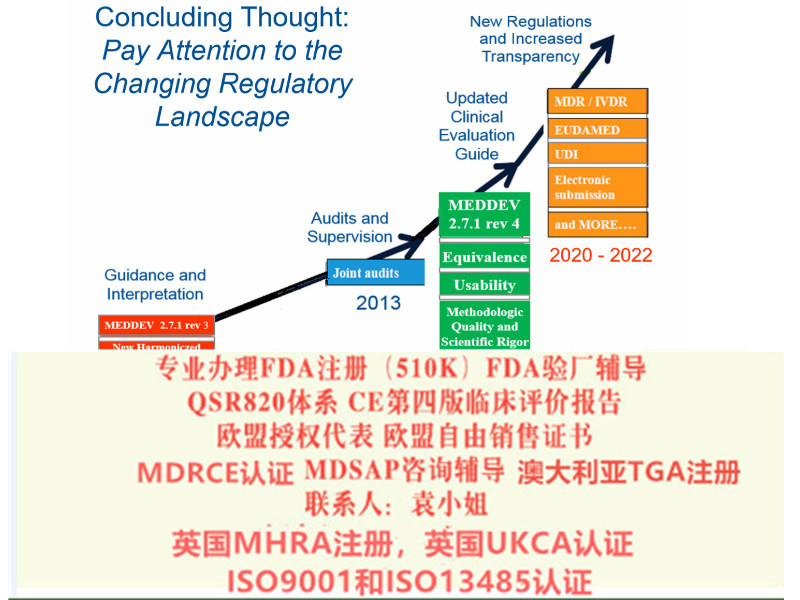
关于欧盟CE 认证的MDR 2017/745法规升级,我们该:
确认原CE的发证机构是否已获得欧盟当局批准的颁发MDR的,目前拥有该的认证机构:BSI、TUV南德(注意TUV莱茵目前还未获得批准);
若要在加拿大销售II类、III类或IV类器械,必须获得加拿大器械许可证(MDL)。MDL是产品批准手续,而MDEL则是对于公司/经销商/进口商的许可。
加拿大器械许可证(MDL)相当于美国食品药品管理局的510(k)许可。 对于II类器械而言,获得MDL的过程通常比获得510(k)的过程快,对于III类器械来说则大致相同,而对于IV类器械来说,前者比后者更加复杂。
加拿大器械与质量管理体系要求。
在申请加拿大器械许可证时,您还需要您已经拥有经过核准、同时也满足加拿大器械法规(CMDR)具体要求的ISO 13485质量管理体系

加拿大MDEL注册
若您计划在加拿大销售器械,您需要进行产品注册登记以获得许可证加拿大颁发两种不同类型的许可证,两种许可分别有不同的要求。

ASTM F2100检测报告
参考标准标准
ASTM F2100现行医用口罩材料性能标准规范Standard Specification for Performance of Materials Used in Medical Face Masks
检测项目及标准
1)过滤效率Bacterial filtration efficiency/ ASTM F2101
2)压差Differential Pressure/ EN 14683:2019 Annex C
3)颗粒过滤效率Sub-Micron Particulate Filtration/ ASTM F2299
4)合成血液穿透Resistance to Penetration by Synthetic Blood
/ASTM F1862
5)阻燃Flammability/ 16 CFR Part 1610
产品注册
制造商在器械投放市场前,应在Eudamed进行注册,提交企业信息及器械信息,包括器械的UDI信息,取得单一注册号(SRN)。
综上所述,持有MDD CE证书的制造商需确认是否有满足过渡条款内提到相关要求,在近一次监督审核前,尽快建立完善相应文件,以保证产品在欧盟市场上的顺畅流通。
我公司办理: 出口英国需要UKCA认证,英国代表,MHRA注册
http://sungofda.cn.b2b168.com









