手动轮椅的MDR CEEU 2017-745认证 EU 2017/745的适用规则 eu2016/425标准
更新时间:2024-12-01 浏览数:1
所属行业:
咨询 管理咨询
发货地址:上海市金山区
产品数量:9999.00个
价格:面议
周期8周
费用100000
资料基本资料
机构SUNGO
产品医疗用品
在此期间,仍然可以进行以下MDD证书的相关活动,例如产品变更及一年期内MDD新户的申请;现有MDD客户证书更新的相关活动;现有MDD客户证书更新的申请(包括提前更新的申请);
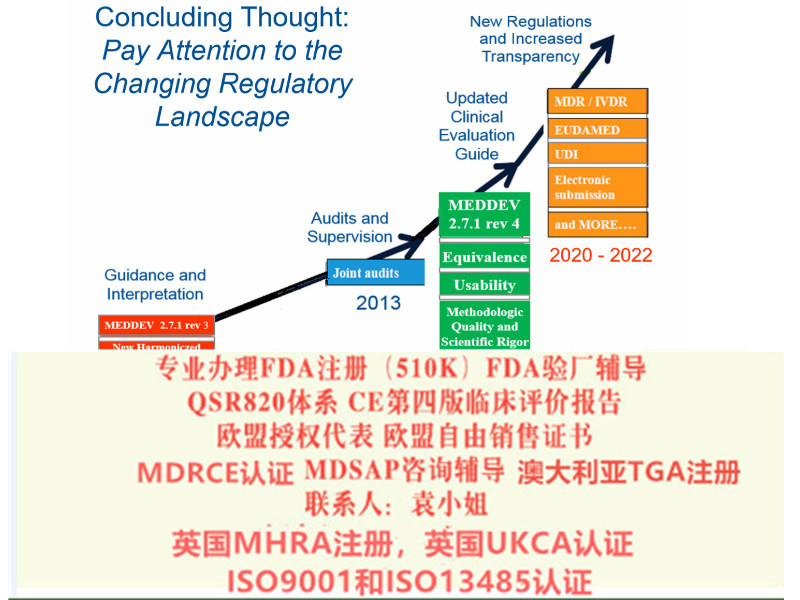
MDR简介 2017年5月5日,欧盟(Official Journal of the European Union)正式发布了欧盟器械法规(REGULATION (EU) 2017/745,简称“MDR”)。MDR将取代Directives 90/385/EEC (有源植入类器械指令)and 93/42/EEC(器械指令)。依据MDR Article 123的要求,MDR于2017年5月26日正式生效,并与2020年5月26日期正式取代MDD(93/42/EEC)和AIMDD(90/385/EEC)。 MDR实施之后,在三年过渡期内仍然可以按照MDD和AIMDD申请CE证书并保持证书的有效性。依据Article 120 clause2 的规定,过渡期内NB签发的CE证书继续有效,但是从其交付日期起有效期不**过5年,并且于2024年5月27日失效。

主要变化之三:评价报告需要有明确的可测量的目标 第四版评估指南对于评估报告的目的有更明确的描述,需要与器械的性、性能以及风险-收益平衡进行更加清晰和详细的描述,在指南的第7部分和附件5中有详细的描述。(袁 () 主要变化之四:确定技术发展水平 第四版评估指南对于设备的技术发展水平和处理方式的建立和文件化,提供了更加详细的描述。这包括确定设备的性和性能,以及被宣称的比对器械,行业的基准器械,或者其他的类似器械;需要包括风险和收益的分析。

关于我国审评审批制度可借鉴的思考 基于对法规的研究,在审评审批及过程中认为有几点值得借鉴: 先是整体的理念,产品符合性评估程序中不仅包含技术文件审评与生产质量管理体系审核,还包含对上市后计划及相关警戒数据报告的审核,且上市后责任明确。在产品上市之前即明确了上市后制造商的责任和义务,并使得上市后有相应的依据。

欧盟授权代表是您与欧洲当局的联系的桥梁,他们必须是在欧洲有实体存在。 欧盟授权代表保存制造商的技术文件,供主管部门检查。 欧盟授权代表的名称和地址必须器械随附的信息上,例如(包装)标签和使用说明。如果发生事故,欧盟授权代表将协助并协调向主管当局报告事件。 MDR下的欧代相比于MDD下的欧代,要求更加严格,责任也更大。除了负有以上义务之外,还会与制造商一样为缺陷器械承担连带的法律责任。另外,授权代表应至少有一名可且持续听其调遣的负责法规符合性的人员,其在欧盟境内的器械要求方面拥有必要的知识。必要的知识应表现为以下任一一种: (a) 在完成有关成员国确认为同等*的法律、、、工程或其他相关科学学科大学*或学习课程后颁发的文凭、证书或其他正式书,以及在体外器械相关法规事务或质量管理体系方面具有至少一年经验; (b) 在法规事务或与器械有关的质量管理体系方面有四年的经验。
加强警戒和市场,一旦器械可以在市场上使用,制造商将必须收集有关其性能的数据,欧盟国家将在市场领域进行更密切的协调。
http://sungofda.cn.b2b168.com