手动轮椅的医疗器械mdr认 什么是MDRCE书 申请要求
发货地址:上海市金山区
产品数量:9999.00个
价格:面议
产地上海
可售地**
品牌SUNGO
型号SUNGO BV
包装纸质
维持质量体系和CE书的有效性。
另外,上市后跟踪的规定,要求制造商主动收集和评估上市后数据,旨在确认器械的有效性、识别之前未知的并已识别的和禁忌症、识别并分析突发风险、确有收益/ 风险的可接受性以及确定器械可能的操作不当或**标示使用以验其预期用途是否正确。上市后跟踪在产品生命周期中的作用不可忽视。

符合性声明中所用的任何通用规范的索引
公告机构的名称和标识号(如适用),所执行的符合性评估程序的说明和所签发的书的标识
如适用,额外的信息
签字人的声明,地址和日期、签字人姓名和职务、以及代签人签名
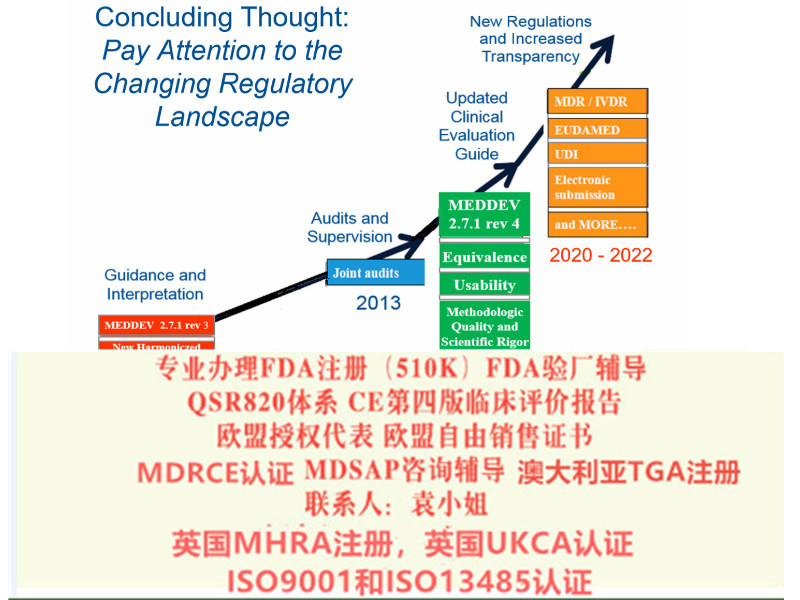
主要变化之六:比对器械
第四版评估指南对于评估器械和比对器械的等效有了更加详细的规定,特别强调对于比对器械的数据的可获得性。需要从数据、技术参数、生物性能三个方面逐一比对,确保所有比对的内容不存在差异。

我司可以办理:
1:欧盟MDR CE,欧盟授权代表,欧盟注册
2:美国FDA注册,FDA510K
3:国内的器械注册和生产许可
4:加拿大的MDEL注册
5:ISO13485咨询和认
SUNGO可以在过渡期内为提供新旧法规的咨询服务,包括:
协助判定产品分类
协助选择合理的符合性途径
协助选择合适的认机构
制定认的解决方案
协助完成评估
编写CE技术文件
欧盟代表服务
http://sungofda.cn.b2b168.com









