周期8周
费用100000
资料基本资料
机构SUNGO
产品医疗用品
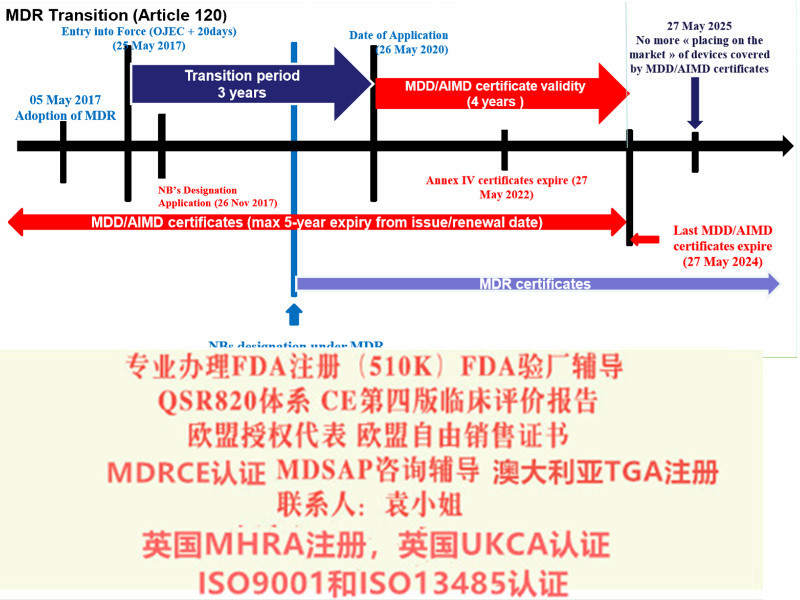
2017 年4 月5 日,欧洲议会和理事会正式签发了欧盟关于器械第2017/七45 号法规(MDR,EU2017/七45),5月5日,欧盟(Official Journal of the EuropeanUnion) 正式发布该法规。2017 年5 月25 日,MDR 正式生效, 替代了原器械指令(MDD,93/42/EEC)和主动植入式器械指令(AIMD,90/385/EEC)。
出口英国需要办理UKCA认证:随着2020 年12 月31 日英国脱欧过渡期结束,2021 年1 月1 日期英国企业器械产品在英国上市,要求符合UKCA 要求。

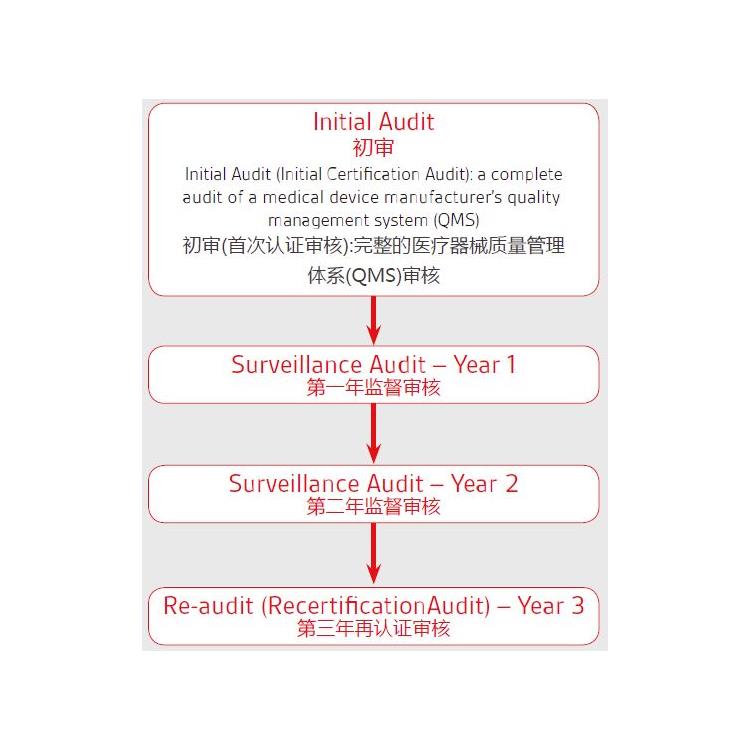
I类无菌器械:
若产品是I类无菌器械,则需要公告机构介入,有一个较长的审核周期。
I类无菌器械销往欧盟要求:
1. 编制产品技术文档
2. 建立ISO13485体系
3. 产品送检,取得产品检测报告
4. 接受公告机构的现场质量体系审核和技术文档审查
5. 获得具备相应的公告机构出具的CE认证证
6. 由欧代在其所在欧盟成员国主管当局(如CIBG、MHRA)进行信息注册并保存制造商的技术文档副
7. 在产品包装、标签上标记带有公告机构号的CE标志
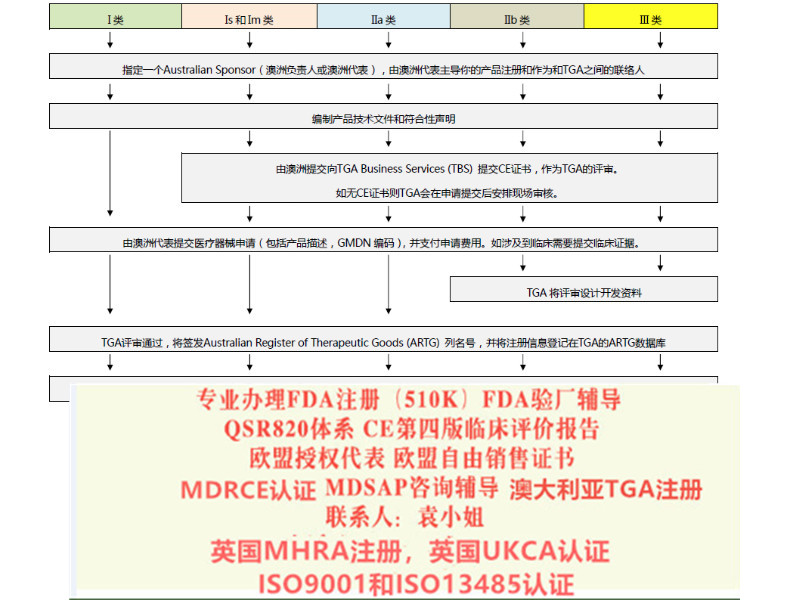
我们的咨询业务 1:MDR法规培训 新法规立法过程、变化及转换期 MDR覆盖的范围,包括和MDD, AIMD的修订要点及主要区别 MDR法规结构及条款清单 MDR分类规则要求 MDR对经销相关方 (Economic Operators)要求 MDR符合性审核程序 质量管理体系的全新要求,以及MDR与ISO 13485:2016的关系 通用和性能要求GSPR MDR对技术文档TCF的要求 评价CER上市后追踪PMCF的要求 上市后监督PMS的要求 MDR中对器械性标识UDI要求; 欧盟符合性声明 (EU declaration of conformity) 要求 器械欧盟数据库(European Database on Medical Devices, EUDAMED)介绍及输入 公告机构的审核准则 充分准备以应对MDR欧盟器械法规相关的审核 Q&A 2:专项,MDR法规变化-UDI和标签 MDR法规变化-GSPR MDR法规变化-PMS、PMCF系统 MDR法规变化-质量管理体系 MDR法规变化-技术文件 MDR法规变化-评估,调查 MDR法规变化-风险管理 可用性评价 3.欧代和注册服务SUNGO 荷兰和德国公司可以提供欧盟授权代表服务,同时提供向当地部门申报注册的服务。 4.整体MDR升级换版实施服务 包含上述1、2、3的全部内容,还包括针对公告机构审核开具的不符合的整改服务。 我们的服务流程 1 预评估:简要管理,以确保清楚了解MDR的重要性和业务影响 预评估考虑组织的挑战:管理意识,人员配备能力和可用性,预算影响 2.差异分析 评估对产品、内部资源、组织和预算的影响 检查新的分类规则(MDR I, IIa,IIb,III类),确认现有和产品的符合性评估路线 核对器械定义,确认是否属于扩大范围或属于附录16中所涉及的属于器械的范围 检查产品与关NB机构有关的要求 审查现有技术文档(技术文件)的变更 评估及更新质量管理体系(以下第3点) 检查可用证据和风险管理的充分性,识别差异(第56条) 评估产品标签(附件I第Il1章) 确保上市后监督的安排充分适宜够(第七章第1节) 制定上市后性能跟踪(PMCF,附件XIV B部分) 做好迎接新的警戒需求的规定(第七章第二节) 确保可追溯相关方面的义务(第3章) 3,质量体系评估 评估新IVDR法规下QMS符合标准和流程的程度 增加新法规应用于QMS的要求 协助和识别合规负责人(PPRC)并参与培训 4,公告机构NB确认 选择合适的公告机构,确认公告机构资质及范围 建立新法规实施过渡计划 5,技术文件编制 编制符合MDR要求的技术文件(TD) 编制评估报告、生物学评价报告和风险管理等技术文件等 产品设计开发流程,确保输入及输出的完整性 确认标签、上市后监督、上市后性能跟踪方案 技术文件整改(风险管理报告,性能评估报告,GSPR等) 6,QMS建立:更新现有体系中IVDR用于QMS的要求 定制企业合规QMS系统 执行体系实施计划确保覆盖各个方面及各方面责任 7, 可追溯性UDI 建立可追溯性QMS要求 建立UDI系统程序及制度 确认UDI的规划及实施

谁必须要申请FDA510(k) FD&C Act的第510(k)规章中并没有特别指出谁必须申请510(k)——任何人都可以申请。但是,他们了哪种行为,例如把器械引入美国市场,要求510(k)申请。基于的行为,必须向FDA递交510(k)的有: (1) 把器械引入美国市场的生产商; (2) 把器械引入美国市场的研发设计者; (3) 改变器械或器械标签的再包装者; (4) 把器械引入美国市场的外国厂家/出口商或外国厂家/出口商的美国代理方
我公司办理:出口美国需要FDA注册,FDA510K,美国代理人(SUNGO可以做510K以及满足FDA要求的510K检测报告,7月份签约价格有优惠)
http://sungofda.cn.b2b168.com