胰岛素注射针CE第四版临床评价报告 新版临床评价报告 需要什么材料
发货地址:上海市金山区
产品数量:9999.00个
价格:面议
周期4周
品牌SUNGO
公司SUNGO
流程SUNGO
国家欧洲
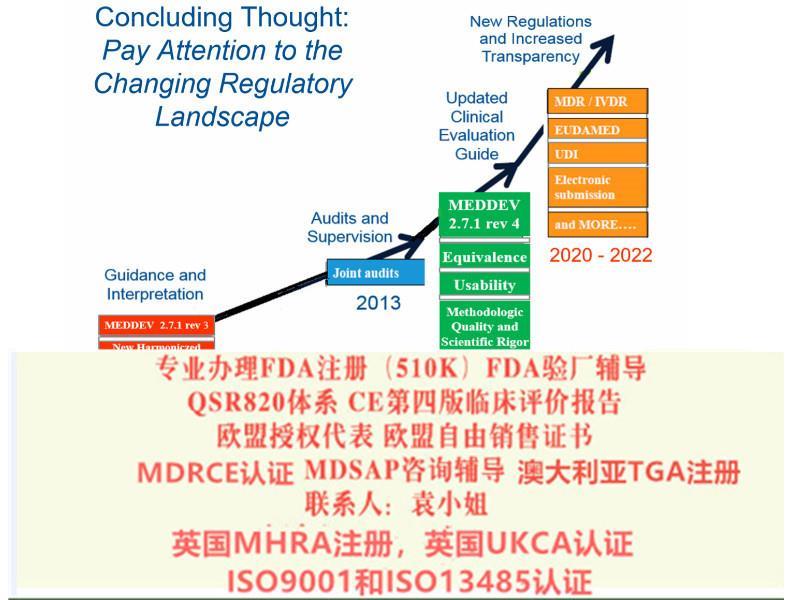
2017年2月Regulation (EU) 2017/745 on Medical Devices器械法规(MDR)提案发布,同年3月,欧盟成员国一致投票表决同意MDR。2017年5月5日,欧盟Official Journal正式对外宣MDR法规内容。
CE第四版评价报告MEDDEV 2.7.1 Rev4难点:
1. 满足要求的比对器械;
2. 筛选文献、评估文献;
3. 应用的背景;
4. 产品的优势

综上所述,持有MDD CE证书的制造商需确认是否有满足过渡条款内提到相关要求,在近一次监督审核前,尽快建立完善相应文件,以保证产品在欧盟市场上的顺畅流通。
加拿大器械机构许可证(MDEL) 假如您生产的是I类器械或IVD,并且不通过经销商而直接销售到加拿大,那么您必须获得器械机构许可证(MDEL)。假如您选择在加拿大通过经销商进行产品销售,那么您的经销商必须拥有MDEL许可证。 无论器械属于哪个类别,器械经销商与进口商都必须获得MDEL许可证。 加拿大器械许可证(MDL)
UKCA 合格评定的要素 UKCA合格评定作为加贴UKCA标志之前不可或缺的一个环节,在器械领域与之前的CE合格评定颇为相似。我们从UKCA合格评定的几个要素来进行展开。

体外诊断器械法规(IVDR)转换期为5年,2022年5月4日起强制实行。MDR将有源器械指令(现行的90/385/EEC)纳入了进来,与一般器械指令(现行93/42/EEC)合二为一,IVDR直接取代了现行的体外诊断器械指令98/79/EEC。主要事项:预计时间英文版MDR及英文版IVDR定稿 ,2017年一月底英文版MDR及IVDR在成员国发布欧盟其他语言MDR 及IVDR在成员国发布 ,2017年2月中欧盟会正式接受MDR及IVDR,2017年3月初欧洲议会正式接受MDR及IVDR,2017年4月初MDR及IVDR正式公开发布,017年4月底MDR及IVDR正式执行 2017年5月底MDR强制执行 ,020年5月底IVDR强制执行 , 2022年5月底MDR CE认证2016年12月14日,EUDAMED(European databank for medical devices) 筹划会上欧盟各国对于器械法规MDR及IVDR的执行进行了一轮的讨论,与会人员对于这两个法规的细节内容进行了讨论并达成了一致意见。
SUNGO服务的宗旨不仅是完成项目,而是帮助客户解决问题并达成目标。
http://sungofda.cn.b2b168.com









