助行器的MDR CEMDR CE EU 2017-745认证 医疗器械法规MDR 完整版
更新时间:2024-09-21 浏览数:7
所属行业:
咨询 管理咨询
发货地址:上海市金山区
产品数量:9999.00个
价格:面议
周期8周
费用100000
资料基本资料
机构SUNGO
产品医疗用品
从2020年5月开始公告机构不能按照MDD颁发CE证,目前I*及以上风险等级产品认证机构已不再受理MDD指令的认证申请。
对于目前获得CE证的企业,应基于自身设备的证据的充分性合理安排申请MDR的时间,尽快启动MDR法规合规准备事宜。
针对MEDDEV2.7.1 Rev 4,我公司可以协助您: 1、寻找等同产品,进行等同分析; 2、搜索文献及其他数据; 3、数据分析; 4、完成评价报告; 5、全英文评估报告; 6、通过公告机构审核。
关于MDR 涵盖产品范围和分类规则 法规对“器械”的定义结合了90/385/EEC 和93/42/EEC 指令的范围,并有所扩大,纳入了有源植入器械、软件以及植入或侵入人体的非用途产品,如、美容植入物、去除脂肪组织的器械、发射高强度电磁进行皮肤等操作的器械、利用磁场大脑元活动的器械等。对药械组合产品的描述也更为具体,法规还适用于使用活性或非活性动物、人源组织或的产品制造而成的器械。 器械的分类仍延续了之前的大类,即按照风险等级分为类:Ⅰ、Ⅱ a、Ⅱ b、Ⅲ类。但分类规则较之前有所增加,由18 条增加至22 条。具体分类规则条款情况及变化情况见下表2:
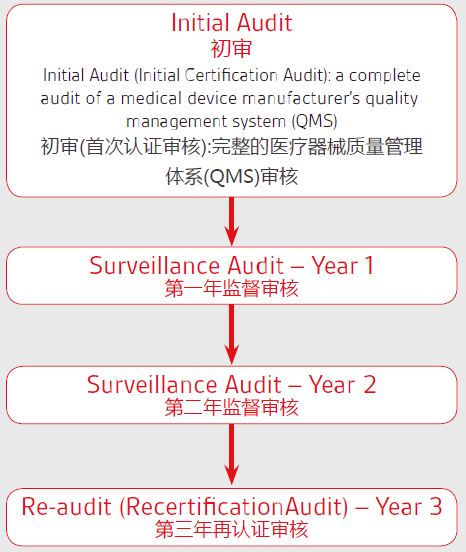
制造商的义务经销商,制造商,进口商等的义务及其关系现已在该条例中明确规定。第10条制造商应有风险管理制度(第2款)和质量管理制度(第9款);进行评估(第3段);编写技术文件(第4段);,并采用合格评定程序(第6段)。制造商亦须对其产品在市场上销售后负责(第12、13、14段)。它们必须有适当的制度来弥补它们对有缺陷的装置造成的损害所负的财务责任(第16段)。每个制造商应一名负责合规的人员(第15条)。一些可植入设备的制造商必须为患者提供植入卡(第18条)。一旦制造商完成所有这些义务,他们应制定一份符合性声明(第19条),并在其设备上应用CE标记(第20条)。欧盟/欧洲经济区以外的制造商应与欧盟/欧洲经济区内的授权代表签订合同(第11条)。授权代表(第11条)、进口商(第13条)和分销商(第14条)的义务也作了明确说明。公告机构NB根据MDR新规定,必须公告机构。器械将被要求满足更严格的标准,特别是在能力方面。

按照附录VIII的规则所划分的器械风险等级 当前声明所涵盖的器械符合本法规,以及适用时其他相关的要求签署欧盟符合性声明的欧盟立法的声明 符合性声明中所用的任何通用规范的索引公告机构的名称和标识号(如适用),所执行的符合性评估程序的说明和所签发的证书的标识 如适用,额外的信息 签字人的声明,地址和日期、签字人姓名和职务、以及代签人签名
我公司办理:出口美国需要FDA注册,FDA510K,美国代理人(SUNGO可以做510K以及满足FDA要求的510K检测报告,7月份签约价格有优惠)
http://sungofda.cn.b2b168.com









