周期4周
包装纸质
品牌SUNGO
是否进口否
可售卖地**
SUNGO致力于为**的器械生产商和经营者提供市场准入的合规咨询以及国际注册服务。
Medical Device Regulation 2017/745/EU法规是什么?
SUNGO集团凭借**网络和队伍为**客户提供法规,帮助企业*贸易壁垒,在器械行业尤为专长。
这主要包括:欧盟CE认证(MDD/MDR)、欧盟授权代表、器械欧盟注册、欧盟自由销售证、FDA注册(FDA510K)、FDA验厂,陪审和翻译、ISO9001/ISO13485,中国局注册证、GMP体系和生产许可证等项目。
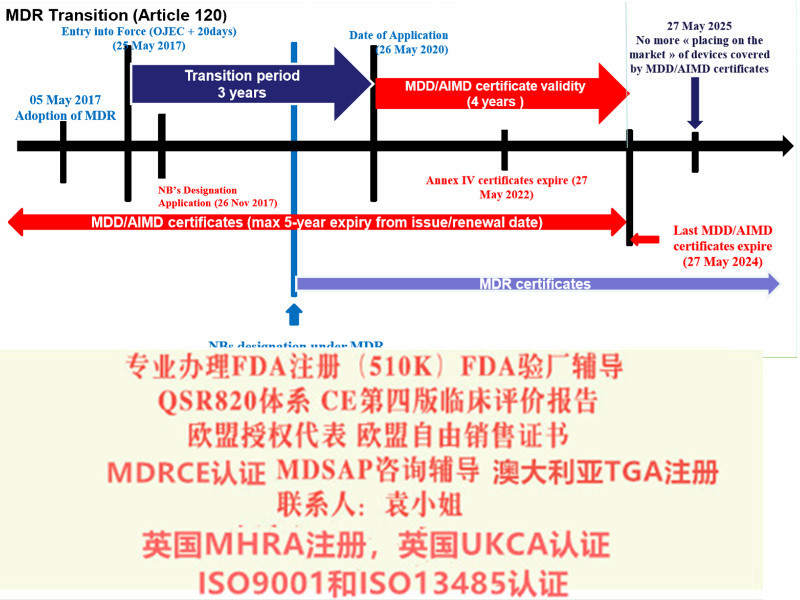
关于欧盟CE 认证的MDR法规升级:
老指令MDD 93/42/EEC including 2007/47/EC 升级到新法规MDR EU 2017/745
2017年5月,欧盟器械新法规MDR (REGULATION EU 2017/745) 颁布,新的法规将替代原有的器械指令 (MDD 93/42/EEC) 和有源植入性器械指令 (AIMDD 90/385/EEC) 。
从2020年5月开始公告机构不能按照MDD颁发CE证,目前I*及以上风险等级产品认证机构已不再受理MDD指令的认证申请。
对于目前获得CE证的企业,应基于自身设备的证据的充分性合理安排申请MDR的时间,尽快启动MDR法规合规准备事宜。

Class I:
1. 为申请Medical Device Establishment License (MDEL)准备相应的技术文件
2. 提交MDEL申请,支付行政收费。
3. 申请评审通过,将在Health Canada网站公示。
Class II:
1. 通过CMDCAS认可的认证机构进行ISO 13485 审核认证(体系审核除ISO13485要求外还要包括CMDR的要求),获得证。
2. 准备Canadian Medical Device License (MDL)申请。
3. 提交MDL申请,并交纳行政收费。
4. Health Canada评审MDL申请, 评审通过后进行网站公示。

加拿大MDEL注册
根据加拿大器械法规(CMDR),按产品风险程度将器械分为 I, II, III和 IV四个等级, 风险等级逐次递增,I类器械为风险,IV类器械风险为。此针对制造者提出的产品注册要求也是逐级增加,要求制造者实行的体系是愈加详尽。
如果您计划进入加拿大市场,则需要进行产品注册登记以获得许可证,加拿大颁发器械机构许可证(MDEL)和器械许可证(MDL)两种不同类型证,并有不同要求
加拿大器械机构许可证(MDEL)
1. 什么是MDEL
MDEL是Medical Device Establishment License 的简称,即器械机构许可证。如果您准备在加拿大生产、进口或分销I类器械,您必须获得加拿大器械机构许可证(MDEL)。MDEL是对于机构的经营许可,无论器械属于哪个类别,器械经销商与进口商都必须获得MDEL许可证。
2. MDEL申请基本流程
(1) 企业为申请Medical Device Establishment License (MDEL)准备相应的文件,
(2) 提交MDEL申请,支付行政收费。
(3) 申请评审通过,将在Health Canada网站公示。
3. 下列几类情况能够豁免 :
(1)零售
(2)企业
(3)在加拿大市场销售企业名下获得器械产品注册证的II类III类和IV类的器械产品的制造厂商 (注:如果是市场销售其他企业名下获得器械产品注册证的II类III类和IV类的器械产品的制造厂商 ,也必须申请办理MDEL )
(4)I类器械产品的制造厂商,根据拥有器械产品营业许可证(MDEL)的企业在加拿大市场销售器械产品 ,则*申请办理MDEL
4. MDEL的有效期限
MDEL没有标明有效期限 ,但MDEL持有者一定要在每年4月1日前递交年度审核申请,MDEL才被视为继续有效,否则MDEL会被撤销 。
MDEL被撤销后,在加拿大的器械市场销售活动则也会被禁止。如果MDEL被撤销 ,MDEL持有者一定要再次申请办理并缴费,才能够再次获得MDEL,申请成功后,会发放一个新的MDEL许可证。
5. 申请MDEL需要完成申请表的如下内容,提交后2-4周可以获得证。
(1) 公司名称及联系方式
(2) 许可文件、邮寄和帐单
(3) 分类和活动表
(4) 场地
(5) 制造商信息
(6)
(7) 签名
选择SUNGO---因为,所以放心!
http://sungofda.cn.b2b168.com