安康帽子的MDRCE认证-需要什么材料
发货地址:上海市金山区
产品数量:9999.00个
价格:¥1234.00 元/个 起
产地上海
可售地**
品牌SUNGO
型号SUNGO BV
包装纸质
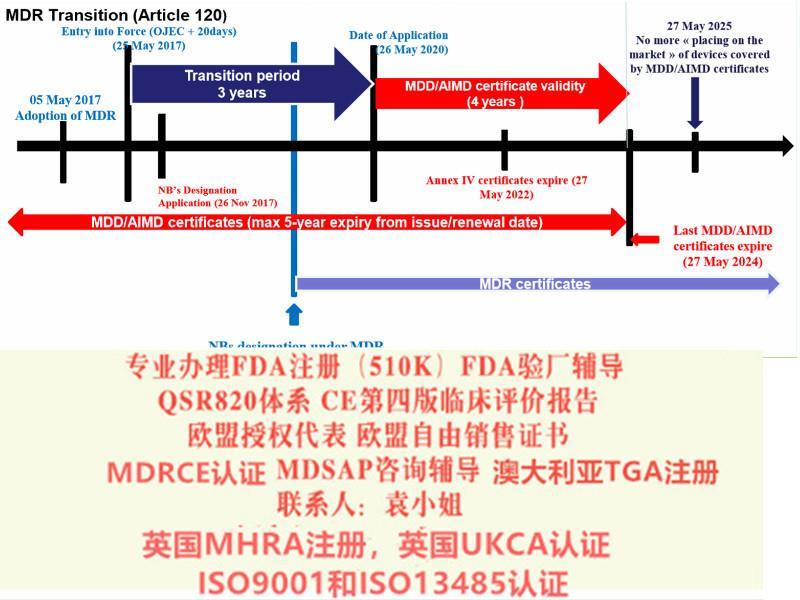
关于欧盟CE 认证的MDR 2017/745法规升级,关于的过渡期:
仅拥有根据指令90/385/EEC和93/42/EEC颁发的的设备可以投放市场,前提是自MDR应用之日起设计和预期用途没有发生重大变化且符合要求新规定。,市场监督,警报,经济运营和设备登记的规定。
针对MEDDEV2.7.1 Rev 4,我公司可以协助您:
1、寻找等同产品,进行等同分析;
2、搜索文献及其他数据;
3、数据分析;
4、完成评价报告;
5、全英文评估报告;
6、通过公告机构审核。

主要变化之九:风险-收益
附件7提供了详细的指南,对于器械的*性和性能表述;
附件7.2 讨论了风险和收益分析,包括对于风险和收益的量的评估,以及总体评价。交付后的数据价值,以及可能会影响统计有效性行的因素等。

主要变化之一:报告更新的频率
按照新版报告指南的要求,对于高风险或者新设备,应每年更新;对于低风险的设备,每2-5年更新。对于如何确定更新的额频率需要有定义。对于任何风险类别的器械,如果从PMS收集到的信息影响到评价或者结论,CER需要进行更新。

2017 年4 月5 日,欧洲议会和理事会正式签发了欧盟关于器械第2017/745 号法规(MDR,EU2017/745),5月5日,欧盟(Official Journal of the EuropeanUnion) 正式发布该法规。2017 年5 月25 日,MDR 正式生效, 替代了原器械指令(MDD,93/42/EEC)和主动植入式器械指令(AIMD,90/385/EEC)。
SUNGO SUNGO Europe B.V. 总部位于荷兰,提供技术服务。主要业务是根据欧洲立法和国际标准,为客户提供完整的技术解决方案。SUNGO集团凭借**网络和队伍为**客户提供法规,在器械行业尤为专长。提供欧盟授权代表服务,可以为客户减少中间环节,节约时间和费用,使您的产品在符合现行欧盟法规的情况下进入市场的程序简单化。
http://sungofda.cn.b2b168.com