参数2
流程1
指令3
费用1
周期4
器械MDRCE认证和MDD指令CE认证区别
现在做出口认证的时候为什么会提到,甚至强调欧代?美代?
FDA注册时,都知道必须授权一个美国代理人,简称美代,可以是美国境内的普通人,也可以是一个企业,但是近年客户对于美代的要求越来越严格,美国境内的普通人远远无法解决企业遇到的问题,而且是经常的联系不上,美代没找好,没遇到问题还好,遇到问题了联系不上,严重的可能会让企业被开出警告信,产品出口受阻,选择一个好的美代很有必要。
欧盟授权代表,在CE认证时很多客户会选择的一项服务,虽然对于那些产品在欧盟法规上属于一类的产品法规规定是不需要加贴欧代信息的,但是现在欧盟对于I以上的 产品是必须加印欧代信息,而很多一类的产品客户也会选择欧代,同等于美代,欧代的重要性也显而易见。
欧代、美代主要是做什么的呢?
欧代、美代就是企业与国外客户联系的纽带,国内外时间差异,产品一旦遇到问题,联系国内需要时间,这个时候就可以联系美代,欧代了,当国外客户不能及时联系国内时,欧代、美代可以帮忙传达,所以,在认证时一定要选择比较有资质,比较好的企业作为自己的欧代。美代,避免关键时间联系不上
欧盟授权代表定义
欧盟授权代表(European Authorized Representative)是指由位于欧洲经济区EEA(包括EU与EFTA)的制造商明确的一个自然人或法人。该自然人或法人可代表EEA的制造商履行欧盟相关的指令和法律对该制造商所要求的特定的职责。
1)提供欧盟授权代表服务的公司是:SUNGO SUNGO Europe B.V. 该公司位于荷兰,为客户提供欧洲法规技术服务。凭借其能力,已经得到了荷兰局的认可提供相关技术服务,同时也被DNV, TUV等国际认证机构认可。目前已经为数百家客户提供了欧盟授权代表服务,为数百家客户提供了欧盟注册服务,同时还为一些客户提供了欧盟自由销售服务。
2)欧盟代表服务内容包括作为企业的联络人,负责处理欧盟市场上所有的客户投诉,、注册等业务。
3)五年有效期内一次清,无年度监督费用。
SUNGO可以在过渡期内为提供新旧法规的咨询服务,包括:
协助判定产品分类
协助选择合理的符合性途径
协助选择合适的认证机构
制定认证的解决方案
协助完成评估
编写CE技术文件
欧盟代表服务
欧代职责:
1. 代表欧盟非制造商与欧盟主管当局打交道
2. 欧盟代表保存新的,贴上CE标志产品的技术文件,确保随时及时的提供给欧盟主管当局审查。
3. 根据非欧盟制造商建立的警戒系统程序,欧盟授权代表协助其进行产品事故报告,召回等
4. 能为客户在欧盟境内销售产品时出现任何问题给予及时的信息沟通与协助解决。
5. SUNGO SUNGO Europe B.V. 总部位于荷兰,提供技术服务。主要业务是根据欧洲立法和国际标准,为客户提供完整的技术解决方案。SUNGO集团凭借**网络和队伍为**客户提供法规,在器械行业尤为专长。提供欧盟授权代表服务,可以为客户减少中间环节,节约时间和费用,使您的产品在符合现行欧盟法规的情况下进入市场的程序简单化。
6. SUNGO SUNGO Europe B.V.作为欧盟代表是被荷兰国家局局认可的。可以帮企业到欧盟主管注册,以免进入海关时出问题和引起法律纠纷,造成不必要的经济损失。
7. 欧盟国家出具的自由销售,目前针对器械做的比较多的是欧盟成员国的局出具的自由销售。SUNGO SUNGO Europe B.V. 可以办理。
我公司办理产品出口欧盟、美国、中东南美等国家的各种认证:
TUV莱茵,TUV南德等CE认证(MDD/MDR法规),CE技术文件编订, CE第四版评价(MEDDEV 2.7.1 Rev 4)编写,欧盟授权代表,欧盟自由销售证书,ISO13485:二016,器械单一审核程序(MDSAP)审核、美国FDA注册(含FDA510K申请),FDA美国代理人服务/ FDA QSR820验厂及整改,FDA警告信应对&RED LIST REMOVAL/QSR820体系/OTC验厂及整改,英国BRC认证咨询,BSCI验厂;口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试、防护服type5/6 (PPE认证咨询(89/686/EC个人防护指令)。

谁可以获得CFS ?
目前欧洲所有的CFS只给位于其境内的公司颁发,这些公司可以是:
1、制造商;
2、欧盟代表;
3、贴牌厂商。
因此中国的制造商要申请CFS证书,只能是通过其欧盟授权代表来完成。
中国制造商申请CFS的条件
1、 了欧盟授权代表,签署了书面协议;
2、 产品有合法性的,这包括:
2. 1、 如果是I类的器械,提供DOC;
2. 2、 如果是I* IIA IIB III类器械,提供公告机构证书。
我公司办理产品出口欧盟、美国、中东南美等国家的各种认证:
TUV莱茵,TUV南德等CE认证(MDD/MDR法规),CE技术文件编订, CE第四版评价(MEDDEV 2.7.1 Rev 4)编写,欧盟授权代表,欧盟自由销售证书,ISO13485:二016,器械单一审核程序(MDSAP)审核、美国FDA注册(含FDA510K申请),FDA美国代理人服务/ FDA QSR820验厂及整改,FDA警告信应对&RED LIST REMOVAL/QSR820体系/OTC验厂及整改,英国BRC认证咨询,BSCI验厂;口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试、防护服type5/6 (PPE认证咨询(89/686/EC个人防护指令)。
SUNGO集团是**化的器械法规技术服务商。
SUNGO包括五家公司,分别是位于美国的SUNGO Technical Service Inc.,位于英国的SUNGO Certification Company Limited,位于荷兰的SUNGO Europe B.V.,位于澳洲的SUNGO Australia 和上海沙格企业管理咨询有限公司。
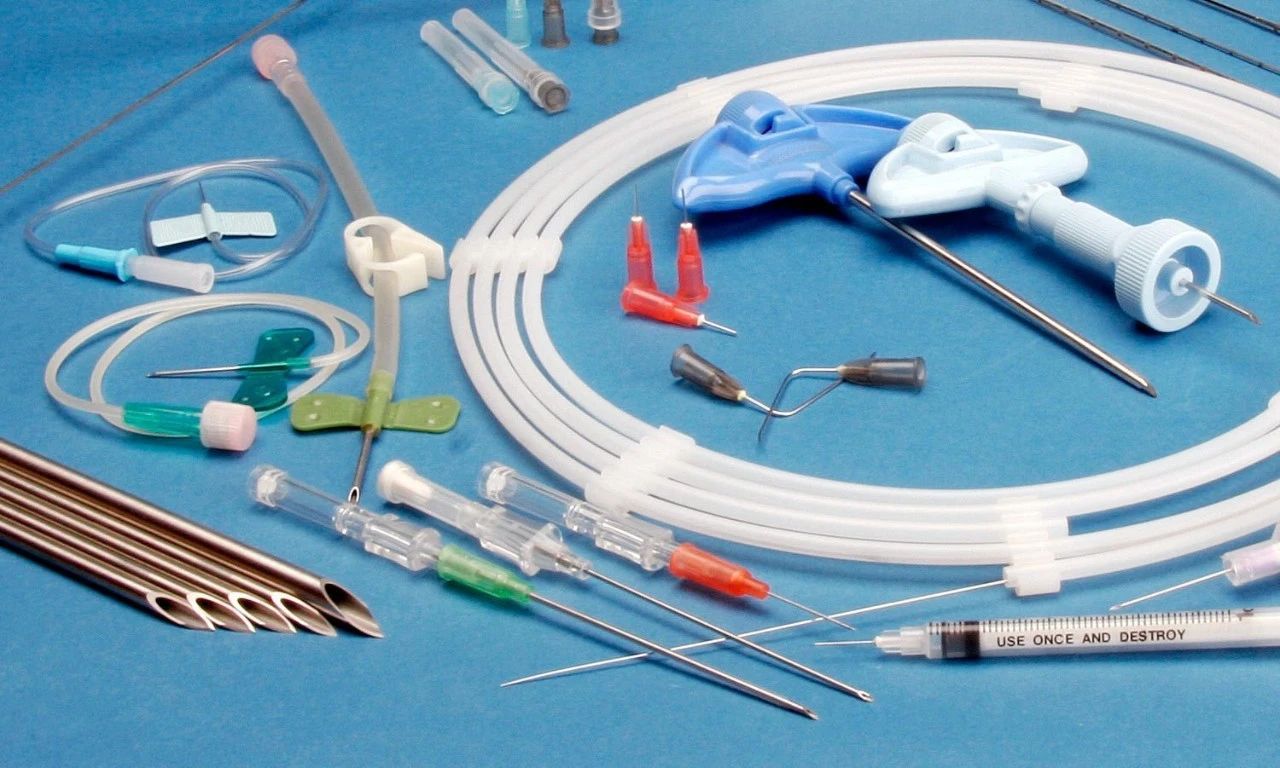
我公司办理产品出口欧盟、美国、中东南美等国家的各种认证:
TUV莱茵,TUV南德等CE认证(MDD/MDR法规),CE技术文件编订, CE第四版评价(MEDDEV 2.7.1 Rev 4)编写,欧盟授权代表,欧盟自由销售证书,ISO13485:二016,器械单一审核程序(MDSAP)审核、美国FDA注册(含FDA510K申请),FDA美国代理人服务/ FDA QSR820验厂及整改,FDA警告信应对&RED LIST REMOVAL/QSR820体系/OTC验厂及整改,英国BRC认证咨询,BSCI验厂;口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试、防护服type5/6 (PPE认证咨询(89/686/EC个人防护指令)。
对于公开文献的数据搜集,国内的生产商还有一个常见的错误,即没有预先建立一个搜索的策略,该策略必须囊括所有适用的数据(无论是正面的还是的),而不是选取仅仅是“好的”文献。在第四版的要求中,仅仅获得数据是没有用的,还需要“运用”这些数据来申请产品的*性和有效性。“运用”包括:
按照第四版原则的要求,评价报告应当包含以下内容:
(一)概要
(二)评价的范围
(三)评价的背景:当前的知识,新的技术水平
(四)评价的设备
4.1评价的类型
4.2等同性说明
4.3制造商产生和持有的数据
4.4来自于文件的数据
4.5数据的总结和审核
4.6数据的分析
(五)结论
(六)下次评价的日期
(七)日期和签名
(八)负责评价的评价者的资质
(九)参考
评价报告还应当确定并论证定期更新的频率:
如果有严重风险或者没有良好的建立风险,则至少每年1次
如果没有严重风险并且已经良好地建立了风险,则2-5年一次
当上市后数据显示对现有的评价有影响时需要主动更新!
CE第四版(MEDDEV2.7.1Rev4)报告
对于生产商的一些建议
1.相比于第三版,第四版给予了更多的指南,生产商应从中*考虑问题力求评估文件完整性和科学性。
2.生产商应关注第四版相比与第三版的差,使评估文件符合新法规的要求。
3.生产商除了关注CE相关法规外,也应关注本国和其他拟出口国家的评估要求。随着国家食品药品监督管理局和CE以及FDA法规当局的沟通利益密切,可以看出局的评估指南,对于CE的评估指南有一定的参考和借鉴意义。
4.生产商应将评估程序纳入质量体系,并应综合考虑拟销售国家的相关试验/评估的法规要求。
关于MEDDEV2.7.1Rev4,SUNGO可以协助您:
1、协助建立评价程序;
2、建立评价方案
3、寻找等同产品,进行等同分析;
4、搜索文献及其他数据;
5、数据分析;
6、完成评价报告。
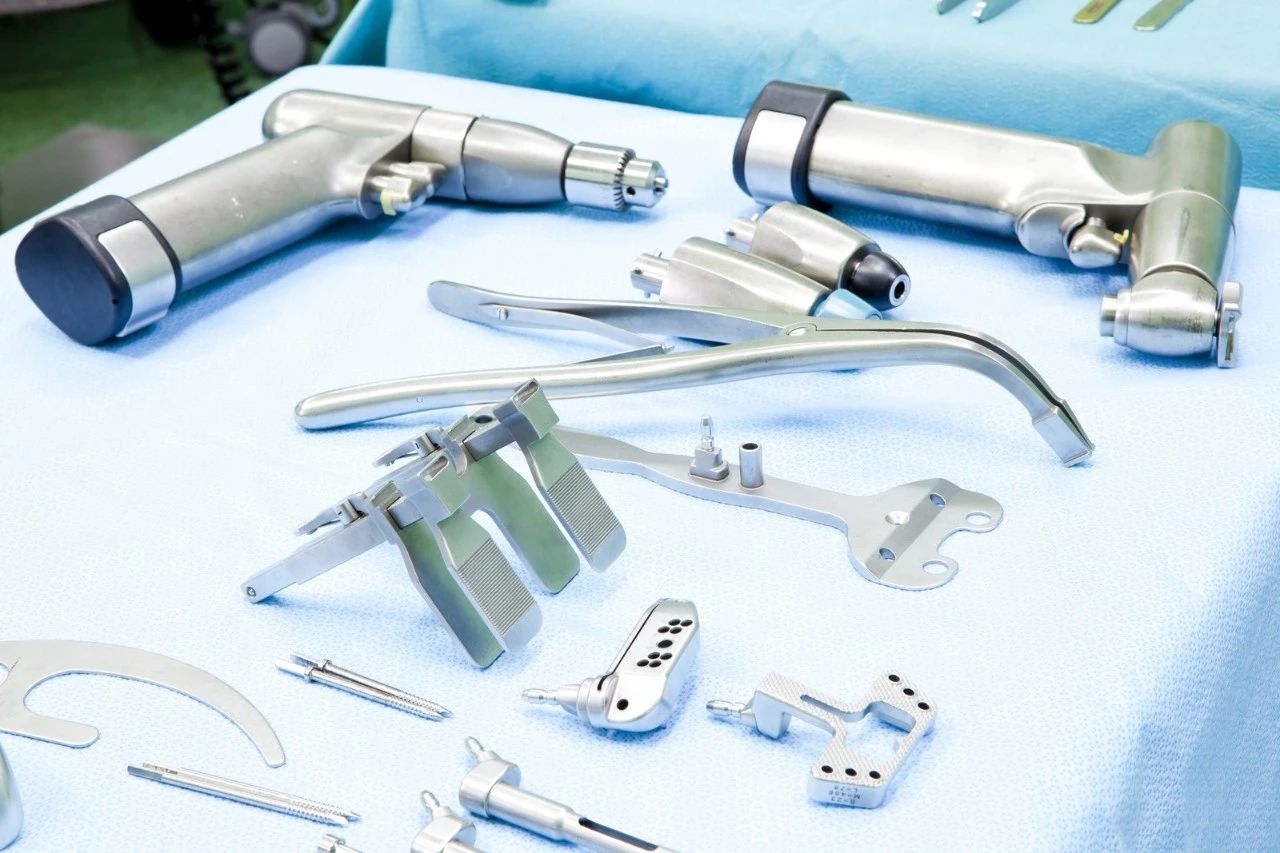
欧盟公告机构,例如TUV南德/TUV莱茵/***/BSI/KIWA/ DNV等公告机构,现在对于新申请CE认证的企业以及已申请过CE认证要进行监督的企业有提出要求,要求企业必须提供第四版评估报告。之前的第三版报告现在已不可用。
制造商应该对第四版进行差距分析,从而:
1)对QMS(质量管理体系)的流程进行影响分析;
2)对CER(现有评价报告)进行差距分析;
3)对实际更新准备过渡计划(过渡计划应考虑与产品相关风险及证书到期日)。
如何更新CER
-上市后监督信息(PMS & PMCF)
-当前技术水平 (State of the art)
第四版评估报告对于第三版而言,变化非常多,更详细,要求更高:
例如对于撰写报告人员有资质要求,必须要有器械行业的法规经验;
对于评估报告的目的有更明确的描述;
对于文献收集要有数据的科学性和有效性;
对于评估器械和比对器械的等效有了更加详细的规定;
对于器械的*性和性能表述;
强调了评估、售后监督和售后评估的关系等等要求,
我公司办理产品出口欧盟、美国、中东南美等国家的各种认证:
TUV莱茵,TUV南德等CE认证(MDD/MDR法规),CE技术文件编订, CE第四版评价(MEDDEV 2.7.1 Rev 4)编写,欧盟授权代表,欧盟自由销售证书,ISO13485:二016,器械单一审核程序(MDSAP)审核、美国FDA注册(含FDA510K申请),FDA美国代理人服务/ FDA QSR820验厂及整改,FDA警告信应对&RED LIST REMOVAL/QSR820体系/OTC验厂及整改,英国BRC认证咨询,BSCI验厂;口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试、防护服type5/6 (PPE认证咨询(89/686/EC个人防护指令)
针对MEDDEV2.7.1 Rev 4,FDASUNGO机构将基于目前申请企业的现状,依据相关要求,编制能够符合发证机构发证公司的全英文评估报告。
1、协助建立评价程序;
2、建立评价方案;
3、寻找等同产品,进行等同分析;
4、搜索文献及其他数据;
5、数据分析;
6、完成评价报告;
7、全英文评估报告;
8、认证机构审核通过。
对于生产商的一些建议:
1.相比于第三版,第四版给予了更多的指南,生产商应从中*考虑问题力求评估文件完整性和科学性。
2.生产商应关注第四版相比与第三版的差,使评估文件符合新法规的要求。
3.生产商除了关注CE相关法规外,也应关注本国和其他拟出口国家的评估要求。随着国家食品药品监督管理局和CE以及FDA法规当局的沟通利益密切,可以看出局的评估指南,对于CE的评估指南有一定的参考和借鉴意义。
4.生产商应将评估程序纳入质量体系,并应综合考虑拟销售国家的相关试验/评估的法规要求。
CMD制造商不需要满足设备标识(UDI)要求。
尽管CMD制造商不需要提供*性和性能摘要(SSCP),但他们必须根据MDR第85条款,为IIa、IIb abd III类器械建立定期*性更新报告(PSUR)或I类器械的报告。
http://sungofda.cn.b2b168.com









