周期8周
费用100000
资料基本资料
机构SUNGO
产品医疗用品
随着MDR(EU 2017/745)法规的实施,欧盟市场对器械的要求越来越高。对于出口量较大的防疫物资——防护服、隔离衣、手术衣,企业有必要了解下各产品出口欧盟需遵循的合规程序。
制造商是否需要一个EAR 为符合上述欧盟设立EAR的要求,中国制造商如果在欧盟成员国或欧盟经济区或双边协议国境内没有商业注册地址,且从事制造出口体外诊断设备、器械、有缘可植入器械等CE指令中要求的产品时,则需要相应法律实体或自然人作为自己的欧洲授权代表。
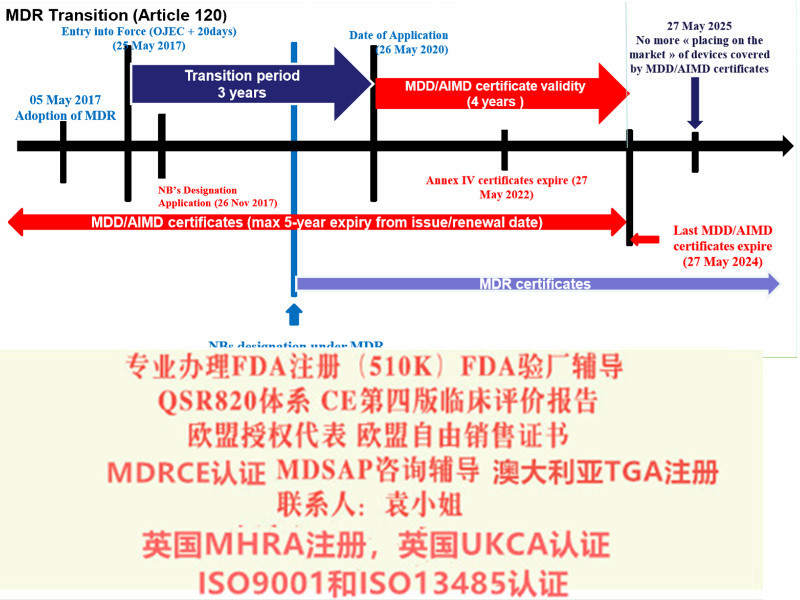
并可在2020 年5 月26 日前并通知符合新法规的符合性评估机构。公告机构可在2020 年5 月26 日前, 采用合规的符合性评估流程并按照新法规签发证书。对于特定Ⅲ类器械和Ⅱ b 类器械产品,在已委派必要的器械协调小组(MDCG)、小组前提下,同样可通过指令豁免在2020 年5 月26 日之前投放市场。法规关于公告机构的要求(正文第35~50 条) 自2017 年11 月26日起适用,即公告机构在新法规发布后的六个月内即应开始进行相应的申请,符合要求后方可依据新法规开展符合性评估。同时法规对成员国主管机构的和MDCG 的成立也设定了期限,要求于2017 年11 月26 日前完成。对于成员国主管机构之间的协调,设定期限为2018 年5 月26 日。

通过更换现行的器械指令(MDD)93/42/ EEC,该新法规将从2020年开始有效。MDR的过渡期MDR法规是2017年发布的,那对于厂家来说,我们还有多长时间来准备呢?
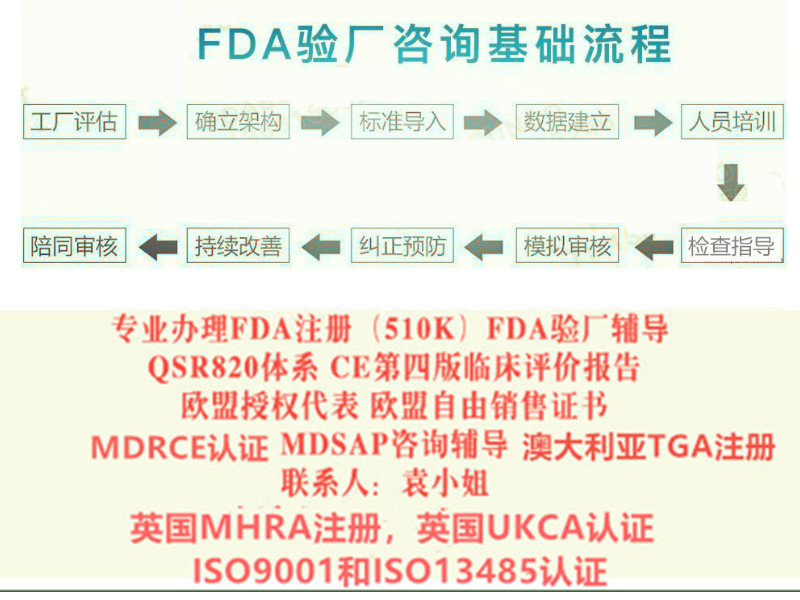
目前急需做CE认证的客户很多,检测认证公司,代理公司也是鱼目混
杂,参差不齐。
怎么辨别口罩CE认证的真假呢?
1,凡是说3、5两千可以出CE证的都是
2,凡是说3/2天可以*的都是
3,凡是说国内公司自己可以发CE证的都是
辨别证的真伪很重要,因为一旦货到了港口清不了关损失就大了。
所以不要贪图*和快而上当受
NB号的CE证。按照现行的欧盟器械法规,此路径获取CE证的
时间至少8个月以上,费用比较昂贵。
欧盟I类器械,如果是非灭菌产品,具体分类为I类。按照指令要求,
公告机构不可强制介入I类器械的发证事宜,制造商可以基于完整的CE技
术文档宣称符合CE(自我CE符合性声明格式如下)。也即,制造商不需
要找发证机构去申请带NB号的CE证,制造商根据自己出具自我CE符
合性声即可打上CE mark,出口欧盟。在欧盟有经销活动前,需要委托
欧盟授权代表去当地主管机构做欧盟注册,整个欧盟28个成员国,只需
登记一次。整个周期是1-4周。
SUNGO服务的宗旨不仅是完成项目,而是帮助客户解决问题并达成目标。所有客户均有专属服务人员,针对市场准入过程中的问题提供的支持和解答。选择SUNGO,不是选择了一次性的合作伙伴,而是选择了一个长期的技术支持的战略伙伴。
http://sungofda.cn.b2b168.com