数量1
长度5
宽2
规格4
质量3
我公司办理产品出口欧盟、美国、中东南美等国家的各种认证:
TUV莱茵,TUV南德,***等CE认证(MDD/MDR法规),CE技术文件编订, CE第四版评价(MEDDEV 2.7.1 Rev 4)编写,欧盟授权代表,欧盟自由销售证书,ISO13485:二016,器械单一审核程序(MDSAP)审核、美国FDA注册(含FDA510K申请),FDA美国代理人服务/ FDA QSR820验厂及整改,FDA警告信应对&RED LIST REMOVAL/QSR820体系/OTC验厂及整改,英国BRC认证咨询,BSCI验厂;口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试、防护服type5/6 (PPE认证咨询(89/686/EC个人防护指令)。
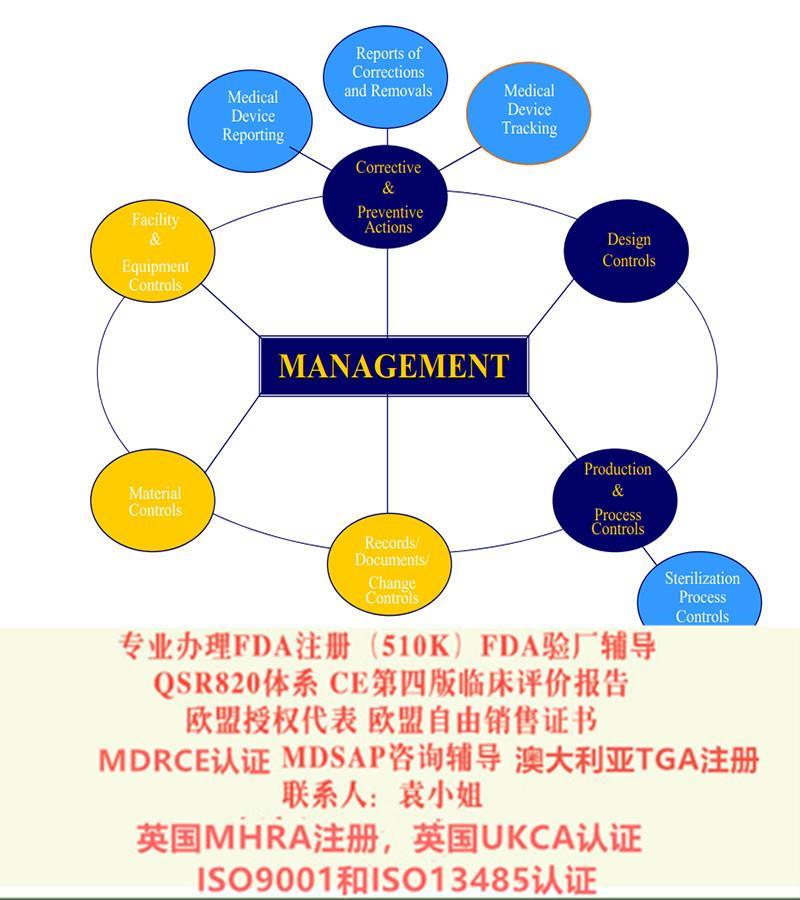
按照MDR法规要求。关键的内容包括如下几个方面:
企业的质量管理体系 EN ISO13485:二016
产品的型式试验 TYPE TESTING
产品的技术文件 TECHNICAL CONSTRUCTION FILES
要满足这些要求,通常需要咨询机构和咨询师的协助。本公司拥有一支经验丰富的咨询师队伍可以为贵司提供这些服务,包括:
协助贵司建立/升级器械质量管理体系,将MDR法规的内容整合进去
协助贵司确定产品的欧盟协调标准,确认检测实验室的资质,样品准备以及检测不合格整改的研讨
按照MDR要求协助贵司准备技术文件,包括风险分析报告,评估资料,基本要求检查表等
协助贵司按照欧盟的要求修订说明书和标签,使其满足出口的要求。
当公告机构现场审核或者文件审核开具不符合时,我们提供整改服务,确*整改验证。
项目背景()
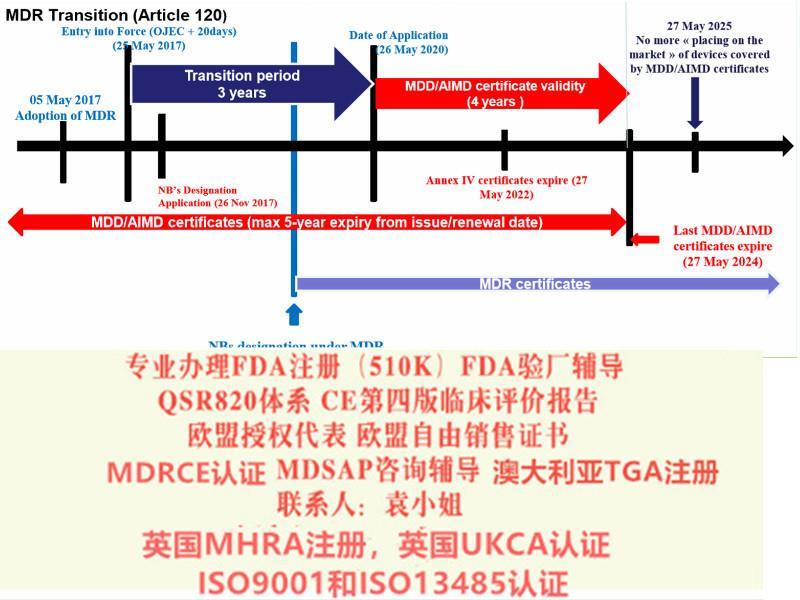
欧洲议会和理事会于2019 年4 月5 日签发的关于器械第2019/七45 号法规, 修订了第2001/八3/EC 号指令,第178/二002 号(EU)法规和第1223/二009 号(EU)法规,并废除了理事会第90/385/EEC 号和第93/42/EEC 号指令.
MDR实施之后,在三年过渡期内仍然可以按照MDD和AIMDD申请CE证书并保持证书的有效性。依据Article 120 clause2 的规定,过渡期内NB签发的CE证书继续有效。至2020年5月26日,MDR法规将*强制实施。至2022年5月26日IVDR法规将*强制实施。至2014年,MDD/ AIMD证书全部失效。
MDR新法规变化
1)扩大了应用范围
2)提出了新的概念和器械的定义
3)细化了器械的分类
4)完善了器械的通用*和性能要求
5)加强对技术文件的要求
6)加强器械上市后的
7)完善评价相关要求
事故对于患者意味着伤害,对于企业的生存也具有巨大的破坏力。因此,评估的设计和数据的收集具有至关重要的意义。然而在实践中,许多制造商不清楚什么是欧盟法规所要求的评估,什么样的数据能满足欧盟的法规要求。
欧盟第四版评价(MEDDEV 2.7.1 Rev 4)指南主要变化
a)报告更新的频率
b)报告编写人和评价人的资质
c)评价报告需要有明确的可测量的目标
d)确定技术发展水平
e)数据的科学性和有效性
f)比对器械
g)比对器械的数据获得
h)什么时候需要试验
i)风险-收益
j)售后监督和售后跟踪
8)提出Eudamed数据库的建立和使用
9)提出器械的可追溯性(UDI)
10)对NB提出严格的要求

英国CFS助力客户产品****数十个
案例二
苏州某生物工程有限公司于2021年9月通过我司申请英国当局签发的三十七份自由销售证书。覆盖到了墨西哥、哥伦比亚、智利、特立尼达和多巴哥、南非、尼日利亚、埃及、加蓬、泰国、危地马拉、多哥、安哥拉、博茨瓦纳、肯尼亚、、阿根廷、塞尔维亚、约旦、沙特、阿尔及利亚、秘鲁、闽台地区、厄瓜多尔、巴西、巴拿马、斯里兰卡、孟加拉、巴基斯坦、阿联酋、以色列、土耳其、黎巴嫩、巴勒斯坦、伊拉克、科威特、卡塔尔和哈萨克斯坦。

我公司办理产品出口欧盟、美国、中东南美等的各种认证:
TUV莱茵,TUV南德,***等CE认证,CE技术文件编订, CE第四版评价(MEDDEV 2.7.1 Rev 4)编写,欧盟授权代表,欧盟自由销售证书,ISO13485:二016,美国FDA注册(含FDA510K申请), FDA QSR820验厂及整改,FDA警告信应对&RED LIST REMOVAL/QSR820体系/OTC验厂及整改,英国BRC认证咨询,BSCI验厂;口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试、防护服type5/6 (PPE认证咨询(89/686/EC个人防护指令)。
欧洲法规部分:欧盟授权代表、MHRA器械注册、CFS 自由销售证、MDD 93/42/EEC 技术文件、IVDD 98/79/EC 技术文件、EN ISO13485:2012导入、验证方案设计和报告编制、GMPC/GMP 认证、净化车间设计及整改、器械欧标检测。
http://sungofda.cn.b2b168.com