周期4周
国家瑞士
有效期1年
费用来电面议
认项目瑞士代表
瑞士也已经不认可欧洲的CE认,您有产品出口瑞士吗?是否有做瑞士代表以及瑞士注册的?
1:手术衣510K,隔离衣510K,手套510K,电动/手动轮椅510K,FDA注册,FDA美国代理人
2:ISO13485认,CE评估报告编写,FDAQSR820等产品出口的相关认
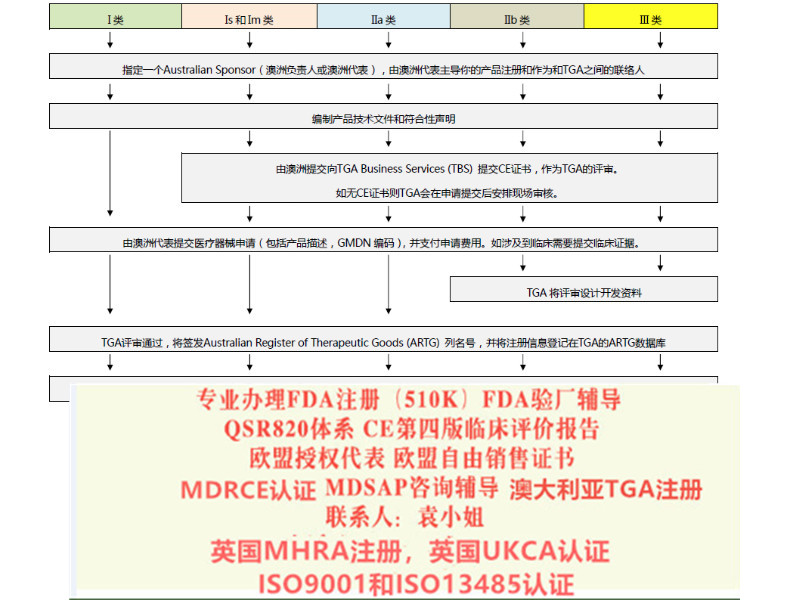
协助判定产品分类
1) I类器械:通常是指不接触人体或只接触完整皮肤的器械。
2) I-m(测量)器械:带有测量功能的I类器械。
3) I-s()器械:终以形式出现在市场上的I类器械。
4) IIa类器械:风险等级较一类器械高,一般是指暂时使用的侵入器械等,有能量交换或测量的有源器械。
5) IIb类器械:风险等级较高,一般指会对人体有潜在风险或者是长时间使用。
6) III类器械:风险等级,一般用于人体循环系统或大脑。
补充:瑞士立后,目前的法规在器械上更趋近于欧盟的MDR法规,而在体外诊断器械上的要求更趋近于IVDD法规的要求。。

瑞士代的职责是什么?
1) 在瑞士境内注册的机构,配备合规负责人PRRC,并完成了CHRN代码的注册;
2) 瑞士代表应和制造商签定书面的瑞士代表协议以约定双方的职责权限;
3) 对投放市场的产品程序和性上合规进行必要的确认,包括检查技术文件、DoC、公告机构书以及注册义务等;
4) 应负责保留制造商的技术文件,当主管当局需要时应在7天内提供;技术文件保留10年,植入性器械保留15年。
5) 及时将投诉和事故信息传递给制造商;确认FSCA以及FSN及时提交给当局;配合当局实施预防措施和纠正措施。

加贴CE产品流通有效期至2024年5月26日;
符合性书有效至2022年5月26日;
经济运营商需在2021年11月26日之前或
投放产品三个月内进行注册
授权代表需在2021年12月31日之前将欧洲
授权代表更换为瑞士授权代表。
在2021年5月26日之前,非欧盟向瑞士出口器械时,需要欧盟授权代表可以满足要求。
但是从2021年5月26日之后,出口瑞士需要单瑞士代表(CH-REP)。
PART1什么是瑞士代表?
瑞士代表的定义:任何在瑞士境内成立的自然人或法人已收到并接受位于瑞士的制造商的书面授权,以代表制造商其在器械条例下的义务的特定任务采取行动。
为了能够履行必要的职责,瑞士代表应其法规负责人PRRC。同时瑞士代表应确保具备充分的知识以应对器械上市前和上市后的各项工作
另外,按照瑞士法规要求,瑞士代表也需要在对瑞士的器械贸易发生后的三个月内完成其CHRN的注册。
瑞士与欧盟的双边协议在2021年5月26日未达成一致而终止。因此从2021年5月26日开始,瑞士的器械管理依据是由其主管当局Swiss Medic在2020年7月1日发布的新版MedDO法规。
沙格为大家准备了瑞士法规系列文章(各主题见文末),一共有五个系列,赶紧收藏!
PART1
新旧版本MedDO法规与MDR/IVDR的关系
目前瑞士器械法规主要是由MedDO的两个版本进行控制和管理,虽然旧版本已经失效,但是新版本有部分内容引用了旧版本,因此需要合并使用。
新旧版本MedDO法规比较
从上表可见,瑞士目前的法规在器械上更趋近于欧盟的MDR法规,而在体外诊断器械上的要求更趋近于IVDD法规的要求。同时,部分新版法规的条款和内容引用了老版本的法规要求。
http://sungofda.cn.b2b168.com









